RayBio高通量抗體芯片助力糖尿病患者傷口修復研究
雜志名稱:EMBO Molecular Medicine
影響因子:14.260
文章題目:Tumor‐associated macrophages‐educated reparative macrophages promote diabetic wound healing
第一作者:母若雨
通訊作者:?董磊,王春明
作者單位:
澳門大學,中藥質量研究國家重點實驗室;
澳門大學珠海澳大科技研究院;
南京大學藥物生物技術國家重點實驗室;
澳門大學健康科學學院生物醫學科學系、藥學系;
本研究所用產品:AAM-BLM-1(可同時半定量檢測小鼠308個因子,包含細胞因子、趨化因子、脂肪因子、生長因子、蛋白酶、可溶性受體、可溶性粘附分子等)
實驗樣品類型:TAMs培養基
摘? 要
糖尿病導致慢性無法愈合的傷口,影響著全世界6000萬人。現有的傷口愈合方法在糖尿病患者中成功率也有限。其原因是在糖尿病患者中啟動愈合的早期巨噬細胞不能正常地轉化為促修復表型所以導致的細胞的功能性障礙。
腫瘤相關巨噬細胞(TAMs)在腫瘤發展過程中會產生豐富的免疫抑制和增殖因子,該研究中研究人員猜測TAMs可以通過細胞因子分泌將其修復功能全部或部分傳遞給非極化巨噬細胞,于是利用TAMs的條件培養基(TAMs - CM)培養正常巨噬細胞,產生巨噬細胞來重現TAMs的修復功能。
TAMs馴化的巨噬細胞(TAMEMs)在體外抑制炎癥、刺激血管生成和激活成纖維細胞方面都優于M0、M1或M2表型的巨噬細胞。且在糖尿病小鼠傷口修復實驗中修復效果顯著。
1
研究結果
1.1 小鼠TAMEMs的制備與鑒定
基于前期研究基礎,該研究挑選了能有效誘導小鼠原代骨髓源性巨噬細胞(BMDMs)中IL-10分泌及I型膠原產生的?S180腫瘤模型。通過活化細胞分選(FACS)后得到TAMs,將TAMs培養15天后收集上清,培養BMDMs,以獲得TAMEMs,同期也經過不同的條件培養基馴化得到M0、M1、M2。
TAMEMs除了形態與其他表型的巨噬細胞不一樣,為細長形態外,其活力也相對保持較高。
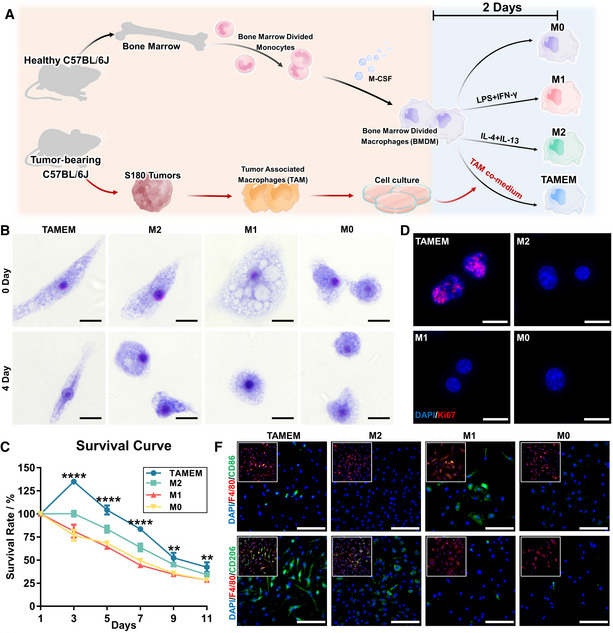
1.2?TAMEMs表現出抗炎和促愈合的表型與鑒定
基因層面,研究者利用RNA‐seq、scRNA - seq分析了TAMEMs與M0、M1、M2的基因表達差異。與M0、M1、M2相比,TAMEMs中表達了更多種類的生長因子和促愈合及抗炎標志物,例如Ccl8和Ccl12等趨化因子,Arg1、Il10、Mrc1等抗炎標志物,Ang、Fgf1、Hgf、Pdgfc等生長因子表達較高,Cx3cr1(糖尿病創面巨噬細胞溶解的重要標志物)。
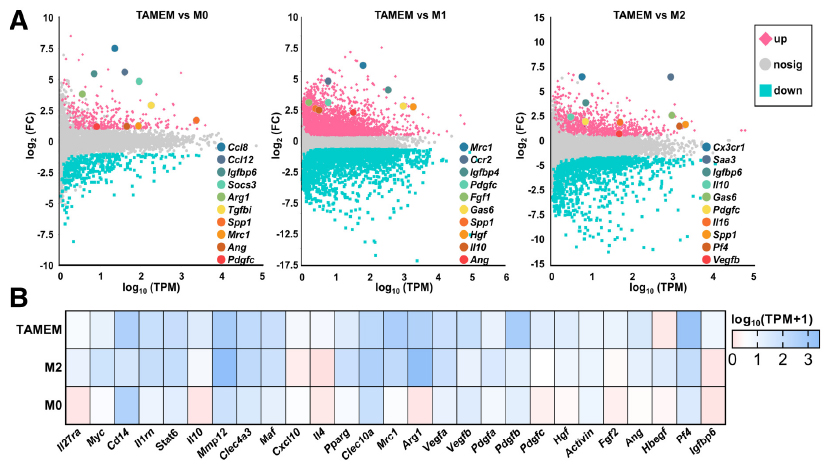


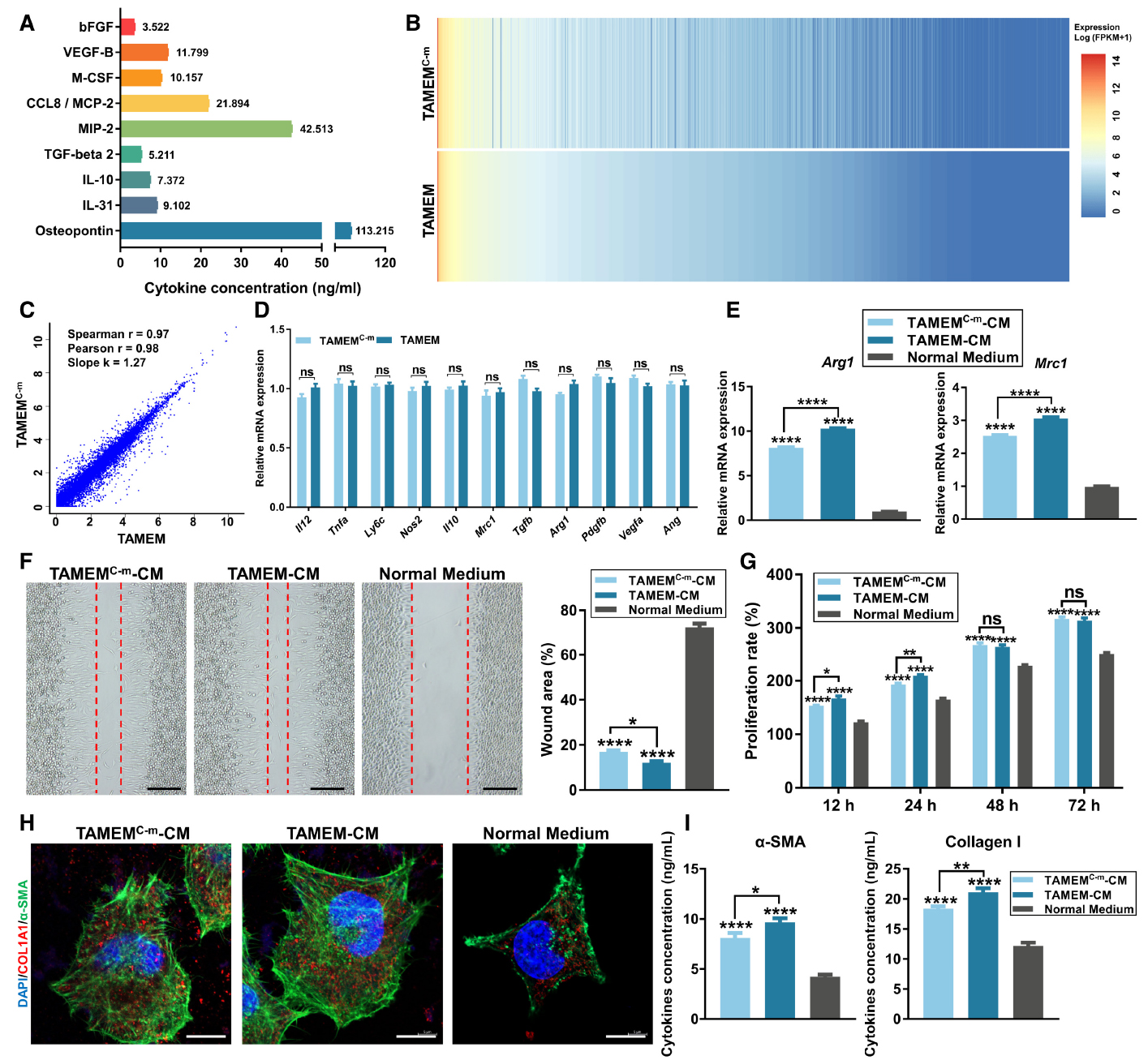
蛋白層面,研究者使用膜芯片[楊1]?分析了細胞因子相關及血管生成相關蛋白,發現TAMEMs分泌了大量的IL – 4及免疫抑制細胞因子/趨化因子,例如IL – 6,bFGF、PDGF - AA和VEGF等促血管生成細胞因子的表達也有所升高,證明了TAMEMs促進組織再生的潛力? 。
評估了TAMEMs對傷口愈合過程中關鍵基質細胞增殖的影響的體外細胞模型實驗Matrigel實驗中,AMEMs‐CM顯示了高效的誘導內皮細胞(SVEC4‐10)形成傷口愈合超過80%(圖3I和J)且TAMEMs‐CM處理的成纖維細胞增殖最快(72小時超過300%;圖3 k)。qPCR、WB和IF實驗中,α‐SMA和I型膠原的表達上調都與膜芯片結果一樣,共同強調了TAMEMs的多面、促愈合功能。

1.3??TAMEMs可以加速I型和II型糖尿病小鼠皮膚傷口的愈合
在小鼠體內移植了TAMEMs后,TAMEMs的存活性良好,且向創面肉芽組織遷移,qPCR檢測Mrc1、Arg1、Cd86和Nos2的表達均在TAMEMs移植小鼠的傷口細胞中表達增加,表明TAMEMs在嚴重炎癥的糖尿病傷口環境中也能維持抗炎表型。
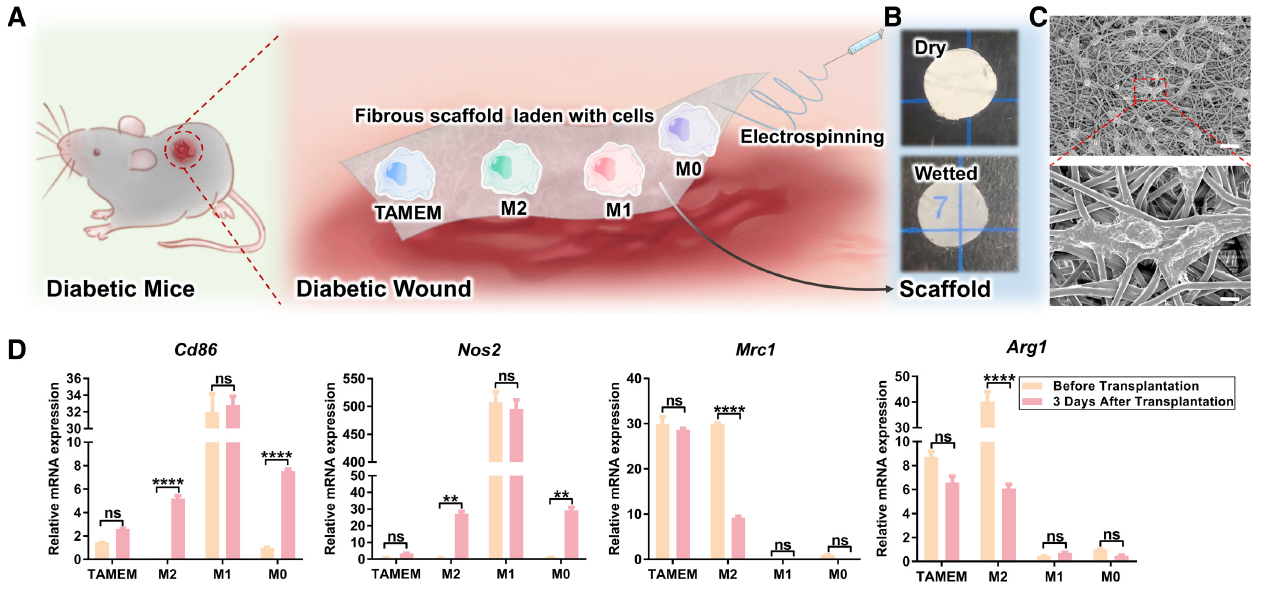
1.4??一種替代由TAMEMs產生的重組TAMs混合物的鑒定
為了避免腫瘤細胞帶來的潛在危害,研究者在不使用任何腫瘤來源細胞的情況下將人巨噬細胞培養成重組型的TAMEMs。首先利用RayBio 能同時半定量檢測308種細胞因子的膜芯片(AAM-BLM-1),分析了TAM‐CM的主要成分,結合前期的膜芯片結果共鎖定了49種促炎、抗炎、集落刺激、趨化和生長等相關因子,最終鎖定了9種蛋白(包括骨橋蛋白(OPN)、IL – 31,IL‐10,TGF‐β 2, M‐CSF, MIP‐2 ,CCL8,VEGF‐B ,bFGF)并通過ELISA測定濃度,添加到RPMI‐1640培養基中形成了重組混合培養基。
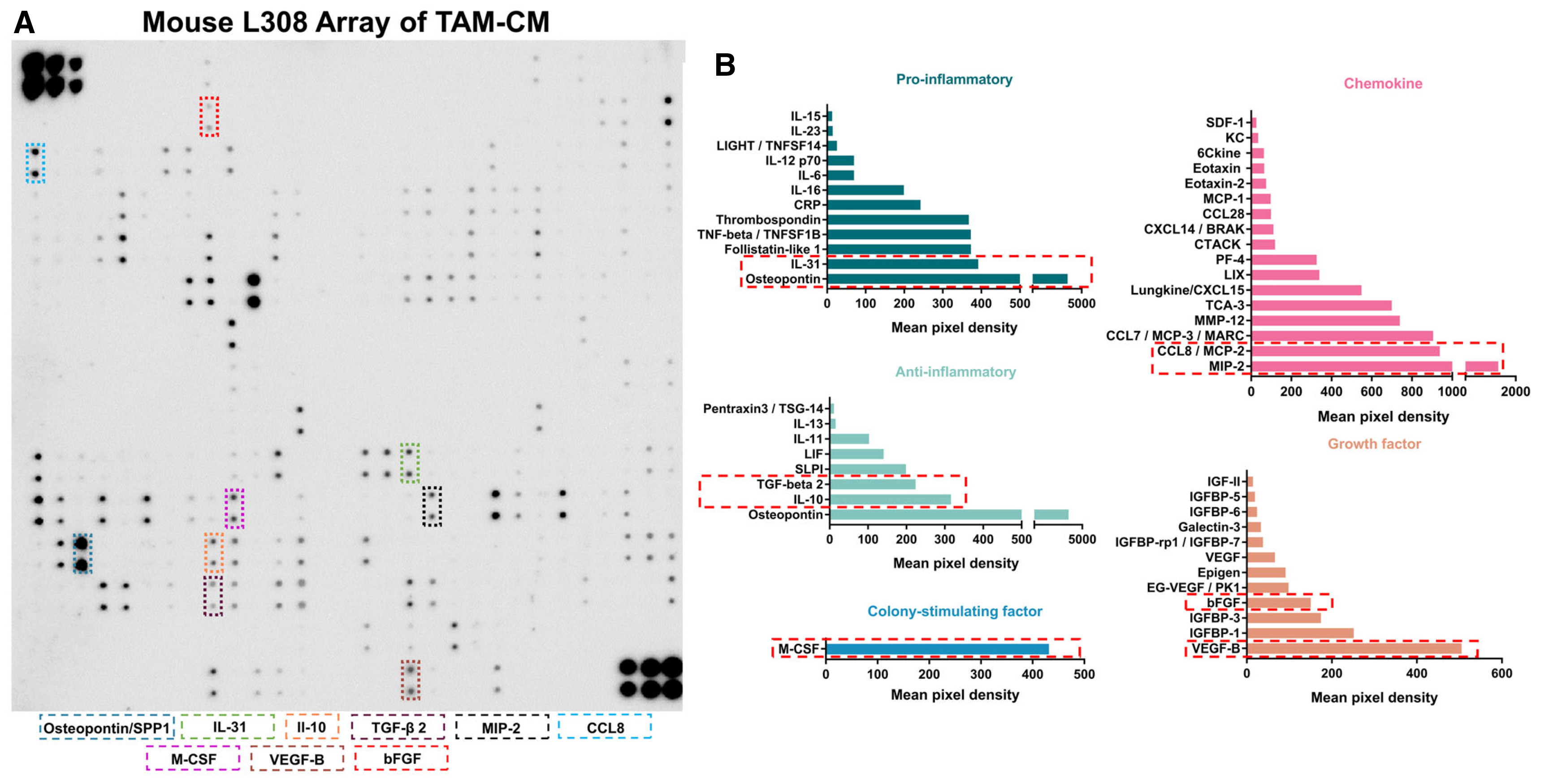
為了評估重組混合培養基培養的TAMEMs(TAMEMsC‐m)的功能,將其用來培養BMDMs,RNA‐seq對比結果發現TAMEMs 和 TAMEMsC‐m在基因表達上高度相似。
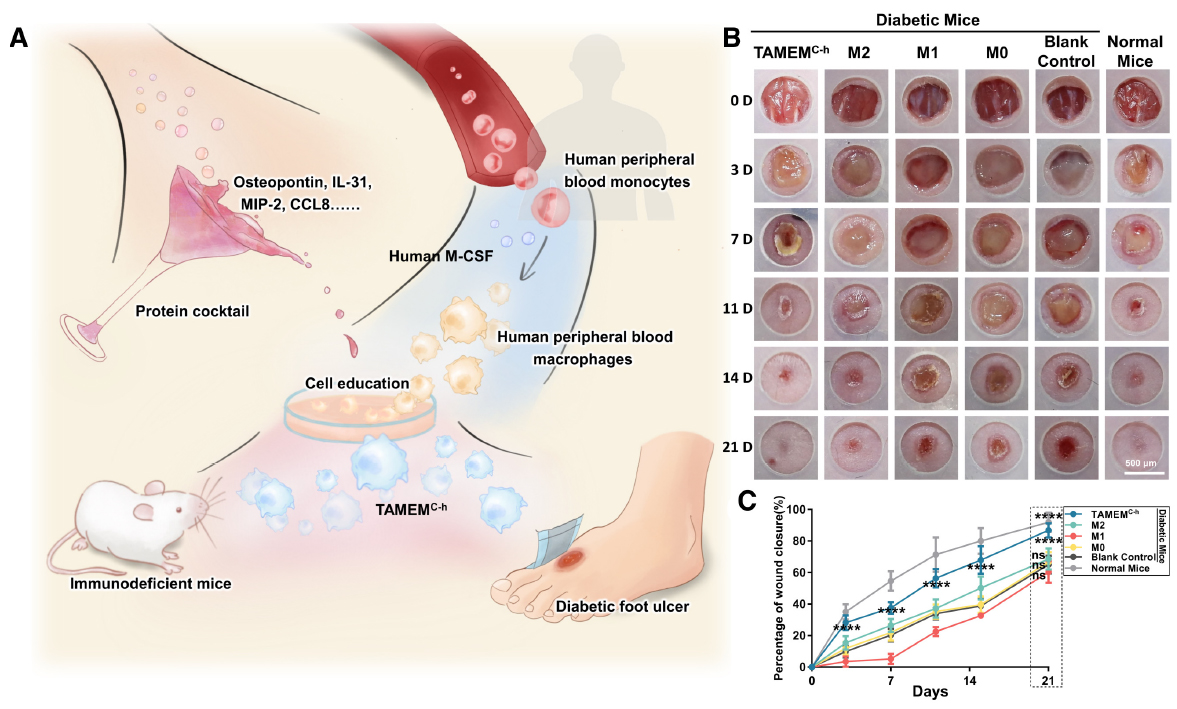
1.5??移植馴化人單核細胞加速糖尿病裸鼠傷口愈合
利用重組混合培養基培養培養從人源單核細胞誘導成的巨噬細胞?(TAMEMsC‐h)?,移植到受傷的免疫缺陷小鼠?(BALB/c nude)中,發現TAMEMsC‐h在 21天的觀察期間改善了愈合。
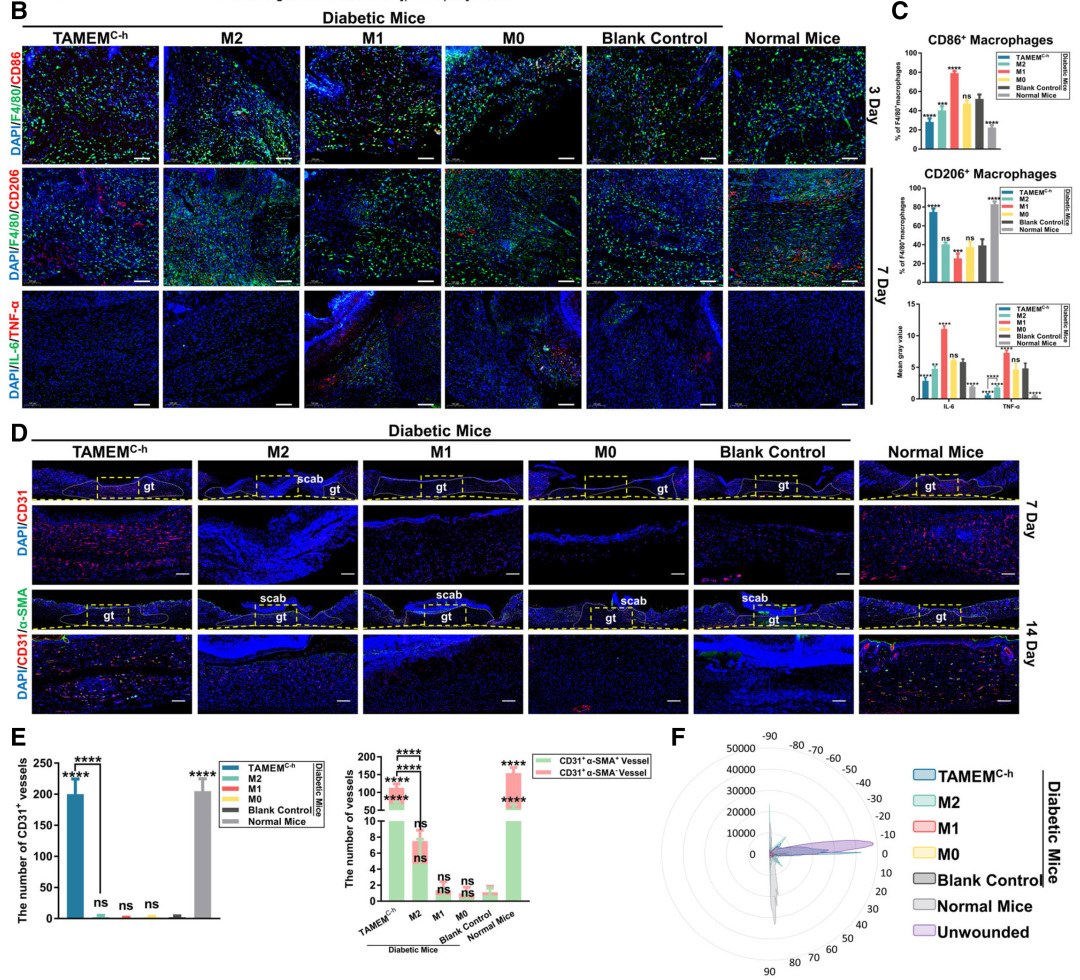
后續研究表明TAMEMsC - h,類似于TAMEMs,在恢復局部免疫平衡和正常血管系統方面發揮了全面的修復作用,使得糖尿病患者傷口愈合效果理想。
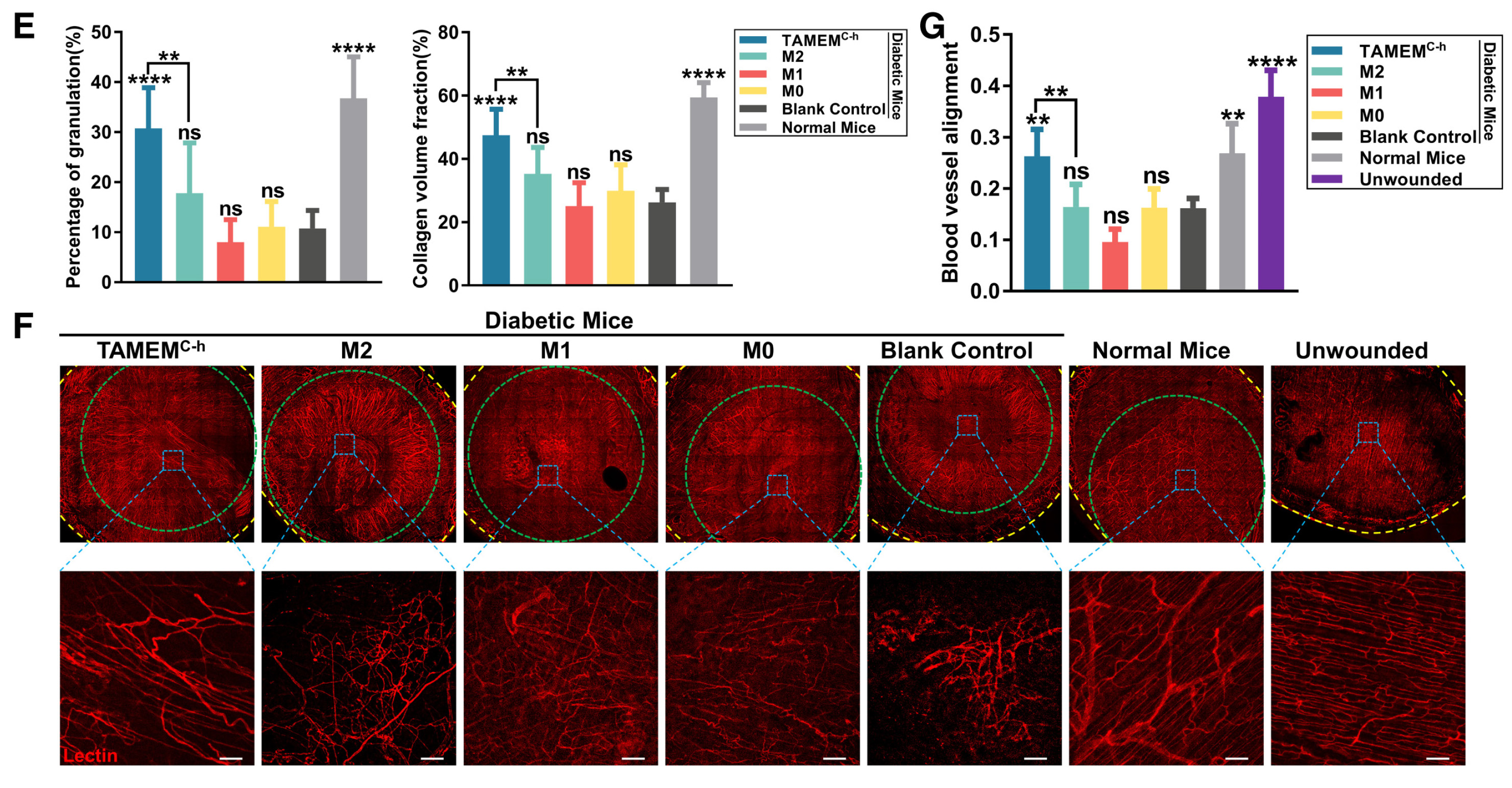
討? 論
本項研究向我們展示了新型巨噬細胞TAMEMs用于糖尿病傷口愈合的制備,通過細胞及體內實驗驗證了TAMEMs在小鼠糖尿病傷口中發揮的關鍵修復活性,包括調節炎癥,刺激血管生成和促進增殖。其中利用RayBio 能同時半定量檢測308種細胞因子的膜芯片(AAM-BLM-1)一次性地對TAMs – CM中的因子含量進行了檢測,快速地鎖定了重組蛋白培養基中關鍵蛋白的含量。

RayBio
Empowering your proteomics






 RayBio資訊
RayBio資訊